 | Информационная система |  |
Государственное санитарно-эпидемиологическое
нормирование
Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных
количеств
ципроконазола и эпоксиконазола в зерне и
масле сои методом капиллярной
газожидкостной хроматографии
Методические указания
МУК 4.1.3134-13
1. Разработаны сотрудниками ГНУ «Всероссийский НИИ защиты растений» (В.И. Долженко, И.А. Цибульская, О.К. Остроухова).
2. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 29 октября 2013 г. № 3).
3. Утверждены врио руководителя Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главного государственного санитарного врача Российской Федерации А.Ю. Поповой 12 ноября 2013 г.
4. Введены впервые.
СОДЕРЖАНИЕ
|
УТВЕРЖДАЮ Врио
руководителя Федеральной службы ________________________ А.Ю. Попова 12 ноября 2013 г. |
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств ципроконазола
и эпоксиконазола в зерне и масле сои методом
капиллярной газожидкостной хроматографии
Методические указания
МУК 4.1.3134-13
Свидетельство о метрологической аттестации № 01.5.04.144/01.00043/2013.
Настоящие методические указания устанавливают порядок применения метода капиллярной газожидкостной хроматографии для определения массовой концентрации ципроконазола в зерне сои в диапазоне 0,025 - 0,25 мг/кг, масле сои - в диапазоне 0,05 - 0,5 мг/кг и эпоксиконазола в зерне и масле сои в диапазоне концентраций 0,05 - 0,5 мг/кг.
Методические указания носят рекомендательный характер.
Название действующего вещества по ИСО: ципроконазол.
Название действующего вещества по ИЮПАК: 1-(1Н-1,2,4-триазол-1-ил)-2-(4-хлорфенил)-3-циклопропилбутан-2-ол.
Структурная формула:
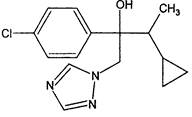
Эмпирическая формула: C15H18ClN3O.
Ципроконазол представляет собой смесь двух диастереоизомеров (в соотношении 1:1).
Бесцветная жидкость.
Температура плавления: 106,2 - 106,9 °С; давление пара при 25 °С: 2,6×10-2 мПа.
Коэффициент распределения н-октанол-вода: KowlogP = 3,1.
Растворимость: в воде - 93 мг/дм3 (22 °С); в гексане - 1,3, метаноле - 410, этаноле - 230, толуоле - 100, октаноле - 100, ксилоле - 120, ацетоне - 360, этилацетате - 240, дихлорметане - 430, диметилсульфоксиде - 180 (все в г/дм3, 25 °С).
Вещество разлагается: 5 % при хранении в течение 2 лет. Вещество стабильно в водном растворе при pH 1 - 9 в течение 35 дней при 50 °С, 14 дней при 80 °С; медленно гидролизуется в 1NHCl и NaOH.
В почвах ципроконазол не аккумулируется и умеренно быстро разлагается, DT50 около 3 месяцев.
Краткая токсикологическая характеристика. Острая пероральная токсичность LD50 для крыс 1020 - 1333, мышей 200 - 218 мг/кг, острая дермальная токсичность LD50 для крыс и кроликов > 2000 мг/кг; не оказывает раздражающего действия на кожу и глаза кролика.
Область применения. Системный фунгицид, действует на грибной патоген внутри растения за счет нарушения процесса биосинтеза стеролов в клеточной мембране.
Гигиенические нормативы для ципроконазола в России. МДУ для сои не установлен.
Название действующего вещества по ИСО: эпоксиконазол.
Название действующего вещества по ИЮПАК: 1-{2-(4-фторфенил)-[3-(2-хлорфенил)оксиран-2-ил]метил}-1H-1,2,4-триазол.
Структурная формула:
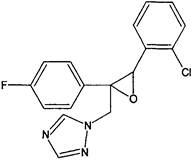
Эмпирическая формула: C17H13ClFN3O.
Эпоксиконазол представляет собой 2R, 3S - 2S, 3R энантиомерную пару.
Бесцветные кристаллы без запаха.
Температура плавления: 136,2 °С; давление пара при 20 °С: 0,01 мПа.
Коэффициент распределения н-октанол-вода: KowlogP = 3,44 (pH 7).
Растворимость: в воде - 6,63×10-4 г/100 см3 (20 °С); в гептане 0,04; ацетоне - 14,4; дихлорметане - 29,1 (г/100 см3).
Вещество не гидролизуется при pH 5 - 7 в течение 12 дней.
В биологически активных почвах эпоксиконазол разлагается почвенными микроорганизмами - DT50 около 2 - 3 месяцев, в растениях экстенсивно деградирует.
Краткая токсикологическая характеристика. Острая пероральная токсичность LD50 для крыс > 5000 мг/кг, острая дермальная токсичность LD50 для крыс > 2000 мг/кг; не оказывает раздражающего действия на кожу и глаза кролика.
Область применения. Системный фунгицид широкого спектра действия, обладает профилактическим и лечебным свойствами, эффективен против возбудителей ржавчины, мучнистой росы и пятнистости на зерновых и сое.
Гигиенические нормативы для эпоксиконазола в России. МДУ для сои не установлен.
1. Погрешность измерений
При соблюдении всех регламентированных условий проведения анализа в точном соответствии с данной методикой погрешность (и ее составляющие) результатов измерений при доверительной вероятности Р = 0,95 не превышает значений, приведенных в табл. 1, для соответствующих диапазонов концентраций.
Метрологические параметры
|
Объект анализа |
Диапазон определяемых концентраций, мг/кг |
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), σr % |
Показатель внутрилабораторной прецизионности, σRл, % |
Показатель воспроизводимости, σR, % |
Показатель точности* (границы относительной погрешности), ±δ, % |
|
ципроконазол |
|||||
|
Зерно сои |
0,025 - 0,25 |
7 |
9 |
12 |
25 |
|
Масло сои |
0,05 - 0,5 |
1 |
8 |
11 |
24 |
|
эпоксиконазол |
|||||
|
Зерно сои |
0,05 - 0,5 |
1 |
9 |
12 |
25 |
|
Масло сои |
0,05 - 0,5 |
7 |
8 |
11 |
24 |
|
*Соответствует расширенной неопределенности Uотн при коэффициенте охвата k = 2 |
|||||
Полнота извлечения ципроконазола и эпоксиконазола,
стандартное отклонение, доверительный интервал
среднего результата для n = 20, Р
= 0,95
|
Анализируемый объект, мг/кг |
Предел обнаружения, мг/кг |
Диапазон определяемых концентраций, мг/кг |
Среднее значение полноты извлечения, % |
Стандартное отклонение, S, % |
Доверительный интервал среднего результата, ± % |
|
ципроконазол |
|||||
|
Зерно сои |
0,025 |
0,025 - 0,25 |
90 |
6,6 |
3,3 |
|
Масло сои |
0,05 |
0,05 - 0,5 |
82 |
7,8 |
3,9 |
|
эпоксиконазол |
|||||
|
Зерно сои |
0,05 |
0,05 - 0,5 |
80 |
9,2 |
4,6 |
|
Масло сои |
0,05 |
0,05 - 0,5 |
76 |
7,9 |
3,9 |
2. Метод измерений
Методика основана на определении ципроконазола и эпоксиконазола в одной пробе методом капиллярной газожидкостной хроматографии с использованием термоионного детектора после их извлечения из образцов зерна сои водным ацетоном, из масла после его растворения в гексане ацетонитрилом и очистки экстракта в системе двух несмешивающихся растворителей.
Идентификация ципроконазола и эпоксиконазола проводится по времени удерживания, количественное определение - методом абсолютной калибровки.
Избирательность метода обеспечивается сочетанием условий подготовки проб и хроматографирования.
3. Средства измерений, реактивы, вспомогательные
устройства и материалы
3.1. Средства измерений
Примечание. Допускается использование средств измерения с аналогичными или лучшими характеристиками.
3.2. Реактивы
|
Ципроконазол, аналитический стандарт с содержанием основного компонента 99,9 % |
|
|
Эпоксиконазол, аналитический стандарт с содержанием основного компонента 99,9 % |
|
|
Азот осч, в баллонах с редуктором |
|
|
Ацетонитрил хч |
ТУ 6-09-3534-82 |
|
Вода для лабораторного анализа (бидистиллят, деионизованный) |
|
|
н-Гексан, хч |
ТУ 6-09-3375-78 |
|
Дихлорметан, хч |
ТУ 6-09-3716-80 |
|
Натрий хлористый, хч |
|
|
Натрий серно-кислый безводный, чда, свежепрокаленный |
Примечание. Допускается использование реактивов с более высокой квалификацией, не требующих дополнительной очистки растворителей.
3.3. Вспомогательные устройства и материалы
|
Воронки делительные объемом 250 и 500 см3 |
ГОСТ 8613-75 |
|
Воронки химические конусные |
|
|
Колбы плоскодонные конические вместимостью 250 см3 |
|
|
Колбы круглодонные на шлифе вместимостью 50, 100 и 250 см3 |
|
|
Ротационный вакуумный испаритель с мембранным насосом, обеспечивающим вакуум до 10 мбар |
|
|
Ультразвуковая ванна с рабочей частотой 35 кГц |
|
|
Фильтры бумажные быстрой фильтрации |
ТУ 6.091678-86 |
Примечание. Допускается применение оборудования с аналогичными или лучшими техническими характеристиками.
4. Требования безопасности
4.1. При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007-76, требования по электробезопасности при работе с электроустановками по ГОСТ 12.1.019-09, а также требования, изложенные в технической документации на газовый хроматограф.
4.2. Помещение лаборатории должно быть оборудовано приточно-вытяжной вентиляцией, соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения по ГОСТ 12.4.009-83. Содержание вредных веществ в воздухе не должно превышать ПДК (ОБУВ), установленные ГН 2.2.5.1313-03 и 2.2.5.2308-07. Организация обучения работников безопасности труда по ГОСТ 12.0.004-90.
4.3. При работе с газами, находящимися в баллонах под давлением до 15 мПа (150 кгс/см2) необходимо соблюдать «Правила устройства и безопасной эксплуатации стационарных компрессорных установок, воздуховодов и газопроводов под давлением» ПБ-03-576-03. Запрещается открывать вентиль баллона, не установив на нем понижающий редуктор.
5. Требования к квалификации операторов
Измерения в соответствии с настоящей методикой может выполнять специалист-химик, имеющий опыт работы методом капиллярной газожидкостной хроматографии, ознакомленный с руководством по эксплуатации хроматографа, освоивший данную методику и подтвердивший экспериментально соответствие получаемых результатов нормативам контроля погрешности измерений по п. 13.
6. Условия измерений
При выполнении измерений выполняют следующие условия:
- процессы приготовления растворов и подготовки проб к анализу проводят при температуре воздуха (20 ± 5) °С и относительной влажности не более 80 %;
- выполнение измерений на газовом хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
7. Подготовка к определению
7.1. Кондиционирование колонки
Перед началом анализа капиллярную колонку кондиционируют в токе азота при температуре термостата колонок 250 °С до стабилизации нулевой линии.
7.2. Подготовка растворителей
Растворители, используемые для анализа, специальной подготовки не требуют. Рекомендуется проверить чистоту применяемых растворителей. Для этого 100 см3 растворителя испаряют при помощи вакуумного ротационного испарителя при температуре 40 °С до объема 1 см3 и хроматографируют. При обнаружении примесей, которые могут мешать определению, растворители очищают общепринятыми методами.
7.3. Приготовление основного и градуировочных растворов
7.3.1. 7.3.2. Основной раствор с концентрацией 0,5 мг/см3: точную навеску ципроконазола или эпоксиконазола (50 ± 0,1) мг помещают в мерную колбу на 100 см3, растворяют в ацетоне и доводят объем до метки тем же растворителем.
Градуировочные растворы ципроконазола с концентрациями 0,5; 1,0; 2,0 и 5,0 мкг/см3 готовят методом последовательного разбавления основного раствора по объему, используя гексан.
7.3.1.1. Раствор № 1 с концентрацией ципроконазола 5 мкг/см3: в мерную колбу на 100 см3 вносят 1 см3 основного раствора и доводят объем до метки гексаном.
7.3.1.2. Раствор № 2 с концентрацией ципроконазола 2,0 мкг/см3: в мерную пробирку вместимостью 10 см3 вносят 4 см3 раствора № 1 и доводят объем до метки гексаном.
7.3.1.3. Раствор № 3 с концентрацией ципроконазола 1,0 мкг/см3: в мерную пробирку вместимостью 10 см3 помещают 2 см3 раствора № 1 и доводят объем до метки гексаном.
7.3.1.4. Раствор № 4 с концентрацией ципроконазола 0,5 мкг/см3: в мерную пробирку вместимостью 10 см3 вносят 1 см3 раствора № 1 и доводят объем до метки гексаном.
Градуировочные растворы эпоксиконазола с концентрациями 1,0; 2,0; 5,0 и 10,0 мкг/см3 готовят методом последовательного разбавления основного раствора по объему, используя гексан.
7.3.2.1. Раствор № 1 с концентрацией эпоксиконазола 10 мкг/см3: в мерную колбу на 100 см3 вносят 2 см3 основного раствора и доводят объем до метки гексаном.
7.3.2.2. Раствор № 2 с концентрацией эпоксиконазола 5,0 мкг/см3: в мерную колбу вместимостью 100 см3 вносят 1 см3 раствора № 1 и доводят объем до метки гексаном.
7.3.2.3. Раствор № 3 с концентрацией эпоксиконазола 2,0 мкг/см3: в мерную пробирку вместимостью 10 см3 помещают 4 см3 раствора № 1 и доводят объем до метки гексаном.
7.3.2.4. Раствор № 4 с концентрацией эпоксиконазола 1,0 мкг/см3: в мерную пробирку вместимостью 10 см3 вносят 2 см3 раствора № 1 и доводят объем до метки гексаном.
Основной раствор можно хранить в холодильнике при температуре 0 - 4 °С в течение 6 месяцев, градуировочные растворы - в течение 2 недель.
Для внесения в образец зерна или масла сои при определении полноты извлечения используют соответствующие градуировочные растворы ципроконазола или эпоксиконазола.
7.4. Построение градуировочного графика
Для построения градуировочного графика (площадь пика - концентрация ципроконазола или эпоксиконазола в растворе) в хроматограф вводят по 1 мм3 градуировочных растворов (не менее 3 параллельных измерений для каждой концентрации, не менее 4 точек по диапазону измеряемых концентраций). Затем измеряют площади пиков и строят график зависимости среднего значения площади пика от концентрации определяемого компонента в градуировочном растворе.
Методом наименьших квадратов рассчитывают градуировочный коэффициент (K) в уравнении линейной регрессии:
|
С = KS, где |
S - площадь пика градуировочного раствора.
Градуировку признают удовлетворительной, если значение коэффициента линейной корреляции оказывается не ниже 0,99.
Градуировочную характеристику необходимо проверять при замене реактивов, хроматографической колонки или элементов хроматографической системы, а также при отрицательном результате контроля градуировочного коэффициента.
Градуировочную зависимость признают стабильной при выполнении следующего условия:
|
|
С - аттестованное значение массовой концентрации определяемого компонента в градуировочном растворе;
СK - результат контрольного измерения массовой концентрации определяемого компонента в градуировочном растворе;
λконт., - норматив контроля градуировочного коэффициента, %. (λконт. = 10 % при Р = 0,95).
8. Отбор проб и хранение
Отбор проб производится в соответствии с «Унифицированными правилами отбора проб сельскохозяйственной продукции, продуктов питания и объектов окружающей среды для определения микроколичеств пестицидов» (№ 2051-79 от 21.08.79), а также в соответствии с ГОСТ 10852-86 «Семена масличные. Правила приемки и методы отбора проб».
Для длительного хранения зерно сои подсушивают при комнатной температуре в отсутствие света. Сухие образцы могут храниться в течение года. Перед анализом пробы зерна доводят до стандартной влажности и измельчают. Пробы масла хранят в холодильнике при 0 - 4 °С в герметично закрытой стеклянной таре не более 2 месяцев.
9. Проведение определения
9.1. Экстракция ципроконазола и эпоксиконазола
9.1.1. Экстракция ципроконазола и эпоксиконазола из семян сои
Навеску измельченного зерна сои (20 ± 0,1) г вносят в колбу вместимостью 250 см3, добавляют 70 см3 смеси ацетон-вода (8:2) и помещают в ультразвуковую ванну на 10 мин. Полученный экстракт фильтруют через бумажный фильтр в круглодонную колбу для упаривания. Экстракцию повторяют еще раз с 50 см3 смеси ацетон-вода (8:2) в ультразвуковой ванне в течение 10 мин. К объединенному фильтрату добавляют 50 см3 дистиллированной воды и упаривают полученный раствор до полного удаления ацетона на ротационном испарителе при температуре бани не выше 30 °С. Водный остаток очищают переэкстракцией по п. 9.2.
9.1.2. Экстракция ципроконазола и эпоксиконазола из масла сои
Навеску масла сои (10 ± 0,1) г помещают в плоскодонную коническую колбу вместимостью 250 см3, добавляют 30 см3 гексана и 100 см3 ацетонитрила, колбу встряхивают и оставляют на ночь. Затем гексаноацетонитрильный раствор переносят в делительную воронку, после разделения слоев гексановый слой отбрасывают. К ацетонитрильному раствору добавляют 50 см3 дистиллированной воды и фильтруют полученный раствор через двойной бумажный фильтр (предварительно смоченный водой) в круглодонную колбу-концентратор. Полученный фильтрат упаривают до полного удаления ацетонитрила при температуре бани не выше 40 °С. Водный остаток помещают на 2 ч в холодильник, затем снова фильтруют через двойной бумажный фильтр (предварительно смоченный водой). Водный остаток очищают переэкстракцией по п. 9.2.
9.2
Очистка экстракта перераспределением в системе
несмешивающихся растворителей
К водному остатку, полученному по пп. 9.1.1 или 9.1.2 и помещенному в делительную воронку на 250 см3, добавляют 10 см3 насыщенного раствора хлористого натрия и экстрагируют ципроконазол и эпоксиконазол дихлорметаном трижды по 30 см3, интенсивно встряхивая воронку в течение 2 - 3 мин. После полного разделения слоев дихлорметановый слой собирают, сушат над безводным серно-кислым натрием (10 г) и упаривают досуха на ротационном испарителе при температуре не выше 40 °С. Сухой остаток растворяют в 1 см3 гексана и 1 мм3 раствора вводят в хроматограф.
9.3. Условия хроматографирования
Газовый хроматограф с термоионным детектором. Капиллярная кварцевая колонка длиной 30 м, внутренним диаметром 0,25 мм с толщиной слоя полярной неподвижной фазы 0,25 мкм. Температура колонки: программирование от 180 °С (1 мин) до 300 °С (4 мин) со скоростью 25 °С/мин. Температура испарителя 300 °С. Температура детектора 380 °С. Расход газов: газа-носителя (азот) - 6,7 см3/мин (170 кПа), водорода и воздуха к детектору - 13 и 200 см3/мин соответственно, дополнительного газа (азот) к детектору - 20 см3/мин, сброс 4,2 см3/мин. Деление потока 1:2,7. Объем конечного экстракта 1 см3, хроматографируемый объем 1 мм3.
10. Обработка результатов анализа
Количественное определение проводят методом абсолютной калибровки. Содержание ципроконазола или эпоксиконазола в пробе (X, мг/кг) вычисляют но формуле:
|
|
Sх - площадь пика определяемого компонента на хроматограмме испытуемого образца, мм2 (AU);
K - градуировочный коэффициент, найденный на стадии построения соответствующей градуировочной зависимости;
V - объём пробы, подготовленной для хроматографического анализа, см3;
Р - навеска анализируемого образца, г;
f - полнота извлечения определяемого компонента, приведенная в табл. 2, %.
Содержание остаточных количеств ципроконазола или эпоксиконазола в образце вычисляют как среднее из двух параллельных определений.
Образцы, дающие пики большие, чем стандартный раствор ципроконазола с концентрацией 5 мкг/см3 или раствор эпоксиконазола с концентрацией 10 мкг/см3, разбавляют гексаном.
11.
Проверка приемлемости результатов
параллельных определений
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает предел повторяемости:
Х1, Х2 - результаты параллельных определений, мг/кг;
r - значение предела повторяемости (r = 2,8σr).
При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
12. Оформление результатов
Результат анализа представляют в виде:
(![]() ± Δ) мг/кг при вероятности Р
= 0,95, где
± Δ) мг/кг при вероятности Р
= 0,95, где
![]() - среднее арифметическое результатов
определений, признанных приемлемыми, мг/кг;
- среднее арифметическое результатов
определений, признанных приемлемыми, мг/кг;
Δ - граница абсолютной погрешности, мг/кг:
|
|
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
В случае, если содержание компонента менее нижней границы диапазона определяемых концентраций, результат анализа представляют в виде:
«Содержание вещества в пробе менее нижней границы определения» (например: менее 0,05 мг/кг*, где * - 0,05 мг/кг - предел обнаружения ципроконазола и эпоксиконазола в масле сои).
13. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-1-6-02 «Точность (правильность и прецизионность) методов и результатов измерений».
13.1. Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из градуировочных растворов.
13.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится с применением метода «добавок».
Величина добавки С∂ должна удовлетворять условию:
|
С∂ = Δл, Х + Δл, Хʹ, где |
±Δл, Х, (±Δл, Хʹ) - характеристика погрешности (абсолютная погрешность) результатов анализа, соответствующая содержанию компонента в испытуемом образце (расчетному значению содержания компонента в образце с добавкой соответственно), мг/кг;
при этом:
|
Δл = ±0,84Δ, где |
Δ - граница абсолютной погрешности, мг/кг:
|
|
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
Результат контроля процедуры Kk рассчитывают по формуле:
|
Kk = Xʹ - X - С∂ |
Хʹ, X, С∂ - среднее арифметическое результатов параллельных определений (признанных приемлемыми по п. 11) содержания компонента в образце с добавкой, испытуемом образце, концентрация добавки соответственно, мг/кг.
Норматив контроля K рассчитывают по формуле:
Проводят сопоставление результата контроля процедуры (Kk) нормативом контроля (K).
Если результат контроля процедуры удовлетворяет условию
|
|Kk| ≤ K, |
процедуру анализа признают удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры к их устранению.
13.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости.
Расхождение между результатами измерений, выполненных в двух разных лабораториях, не должно превышать предел воспроизводимости
|
|
(3) |
X1, Х2 - результаты измерений в двух разных лабораториях, мг/кг;
R - предел воспроизводимости (в соответствии с диапазоном концентраций), %.